COPD中的膈肌肌纤维功能障碍(Part 1)
【摘要】
COPD患者的吸气肌无力具有重要的临床意义。对于严重COPD患者,最大吸气压是生存的独立决定因素。传统观点认为,吸气肌无力源自肺气肿导致的膈肌缩短。但近期研究发现,膈肌细胞和分子结构的改变可能是其病理本质。COPD患者膈肌纤维类型转变,Ⅱ型纤维转化为Ⅰ型纤维,使得膈肌的抗疲劳性更好,但同时膈肌肌力下降,可能导致膈肌无力。膈肌肌纤维产生的肌力下降与肌球蛋白含量降低有关。此外,COPD患者的膈肌存在氧化应激损伤和肌节损伤,这可能激活蛋白水解机制,引起收缩蛋白萎缩,进而导致膈肌纤维产生肌力的能力下降。有趣的是,这些病理改变在COPD早期(GOLDⅠ/Ⅱ)即已出现,即使患者尚未见日常活动能力下降。因此,针对轻-中度COPD患者膈肌功能的体内研究将是未来研究的重点。针对COPD膈肌功能障碍的治疗是复杂的,因为其病因仍不明确。但近期研究显示,对于肌肉萎缩(例如膈肌)的相关症状,蛋白酶体抑制剂具有良好前景。
【COPD膈肌的分子和细胞学改变】
1.膈肌纤维类型转变为氧化性Ⅰ型纤维
研究已证实,严重COPD患者的Ⅰ型纤维(慢收缩、抗疲劳纤维)比例增加,Ⅱ型纤维(快收缩、疲劳纤维)减少。亦有研究提示,这种转变在轻-中度COPD患者中已经发生。
2.COPD膈肌单纤维的功能障碍
a)收缩功能
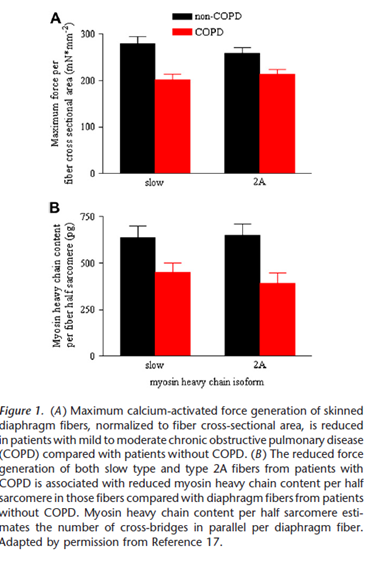
Levine等的研究显示,严重COPD患者膈肌去膜纤维产生的肌力下降35%。我们的研究显示,这种下降在轻-中度COPD中也非常明显(25%)。肌纤维产生的最大肌力主要取决于肌球蛋白含量。COPD膈肌纤维的最大肌力下降与肌球蛋白含量降低30%相关(见Figure 1)。
最近的研究显示,在一定钙浓度下,COPD患者膈肌肌纤维产生的肌力/最大肌力小于非COPD患者,这提示,维持同样的肌力,需要更高的胞浆钙浓度,因此,Ca2+-ATP酶消耗的ATP更多。或者,在亚极量激活时,钙敏感性下降会影响膈肌肌力。
b)被动张力下降
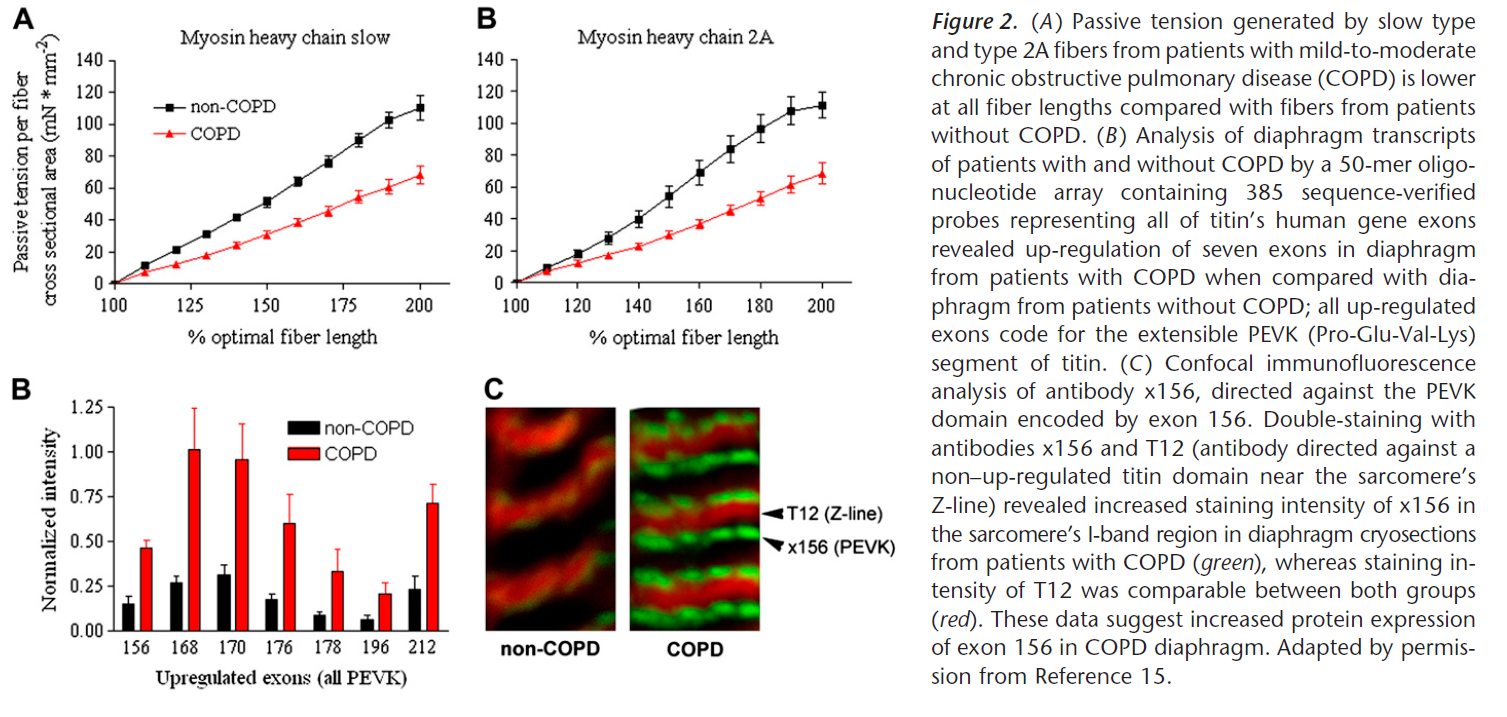
为达到最佳收缩功能,肌节的被动弹性结构是必不可少的。与无COPD者比较,轻-中度COPD患者膈肌纤维牵拉时的被动张力更低。膈肌纤维的被动张力主要取决于肌联蛋白的特性。在COPD患者膈肌中,肌联蛋白的弹性结构区域PEVK(Pro-Glu-Val-Lys)外显子编码表达增加,导致肌联蛋白弹性片段延长,从而降低膈肌纤维的被动张力(Figure 2)。
3.膈肌萎缩:并不仅限于严重COPD
横截面积并不是肌肉萎缩的敏感指标。与无COPD的患者相比,严重COPD患者的膈肌纤维横截面积更小,但是这一差异未见于轻-中度COPD患者。而近期数据显示,轻-中度COPD患者Ⅰ型和Ⅱ型膈肌纤维中,均可见肌球蛋白显著减少(~30%),但肌纤维横截面积未见改变。肌球蛋白减少,单位横截面积产生的最大肌力下降。
4.COPD中的膈肌损伤
轻-中度COPD膈肌横截面未见损伤,但肌节长度变短。中-重度COPD患者,可见肌节断裂和Z线错位,出现内核和小角纤维,在对抗吸气负荷时更易导致肌节断裂,其敏感性较无COPD患者升高三倍。COPD急性加重时,膈肌负荷增加,肌节损伤增加,进一步削弱膈肌功能,最终导致呼吸衰竭。
Leo Heunks系列(8):COPD中的膈肌肌纤维功能障碍(Part 2)
【COPD膈肌病理生理学改变】
COPD膈肌肌纤维类型的转变被认为是有益的,因为膈肌抗疲劳能力更强。事实上,严重COPD患者在最大通气时并未见膈肌疲劳,在力竭运动后膈肌疲劳也不常见。相反,膈肌单纤维的肌球蛋白减少、肌力产生能力下降,肌节损伤和氧化应激,是膈肌的病理性改变,将显著削弱膈肌肌力。
1.COPD患者的膈肌无力:体内vs体外
Levine等基于去膜纤维收缩力的数据来计算最大跨膈压,结果显示,严重COPD患者的最大跨膈压约为正常值的60%。膈肌细胞和分子水平的改变完全可以解释膈肌力量的下降。事实上,在同等肺容量时,部分COPD患者的最大跨膈压还高于健康受试者。但需要注意的是,胸腔内负压和跨膈压是吸气肌力量的间接测量方法(这些测量方法不仅依赖于肌肉功能,还与神经功能和神经肌肉传导功能密切相关),而体内直接测量膈肌收缩能力的方法难以获得。因此,为了阐明体内与体外膈肌功能的差异,有必要测量轻-中度COPD患者的跨膈压,同时联合评估中枢驱动、神经功能和神经肌肉传导。
2.COPD患者的膈肌萎缩:蛋白水解、氧化应激、肌节损伤之间的关系
目前观点认为,蛋白水解加速(通过泛素-蛋白酶体途径)导致COPD膈肌肌球蛋白丢失,是膈肌无力发病机制的第一步。
COPD患者在吸气负荷时,易导致额外的膈肌肌节损伤。肌联蛋白可将粗肌丝维持在中心位置,在维持肌节的结构和机械稳定性方面发挥主要作用。肌联蛋白的刚性下降,可能引起膈肌肌节结构失去稳定,导致粗肌丝错位和无法应对肌节长度不均。严重COPD患者中,这种肌节的过度拉伸可能导致膈肌肌节损伤。
此外,我们推测,在严重COPD患者的膈肌肌节中,氧化蛋白含量升高,会导致膈肌损伤的敏感性增加。氧化蛋白的结构完整性和功能被破坏,被认为是蛋白酶体降解的底物。这些微小的结构改变可能已经存在于轻-中度COPD患者,且通过加速蛋白酶体介导的蛋白水解,导致收缩蛋白功能障碍和肌球蛋白丢失。
3.COPD膈肌损伤后的再生?
肌肉损伤通常伴随炎症反应,随后可见肌肉再生,以防止肌肉量的丢失。虽然COPD患者存在广泛而明显的膈肌纤维损伤,但并未见炎症细胞的浸润。Nguyen等发现,严重COPD患者中,胚胎/新生肌球蛋白重链(MHC)表达减少。正常情况下,肌肉损伤和再生时可见MHC增加,因此COPD患者的胚胎/新生MHC应增加。虽然仍有待探讨,目前的数据提示COPD患者膈肌损伤后的再生反应并不充分。肌肉损伤后再生的关键特征是:卫星细胞激活,增殖为成肌细胞,最后分化为新的肌肉组织代替损伤/变性的组织。未来的研究重点应是了解卫星细胞的增殖和分化能力。
4.COPD膈肌蛋白合成减少
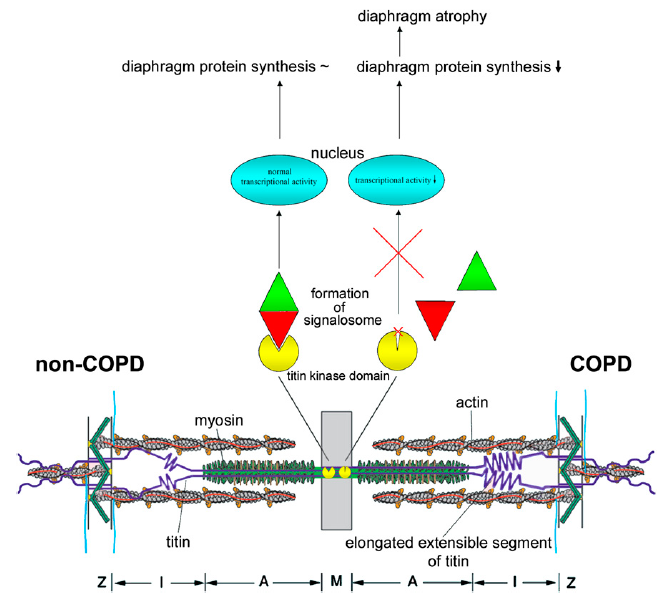
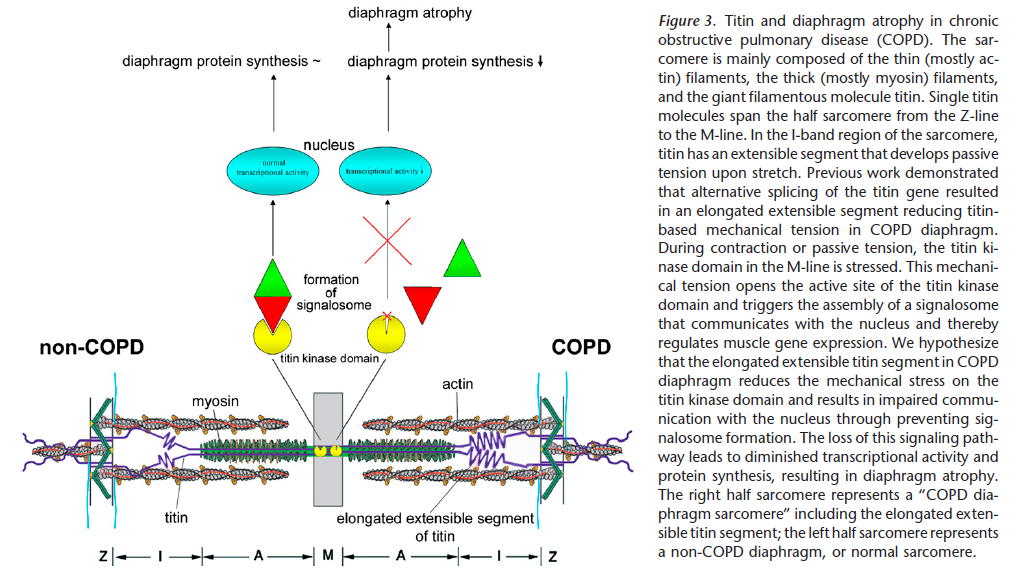
肌联蛋白对于维持肌肉量非常关键。此外,肌联蛋白具有牵张感受器功能,肌联蛋白的刚性可调节肌肉重塑和基因表达(通过一个信号通路,来连接肌联蛋白激酶结构域的活性和细胞核转录活性)。在早期发展为呼吸衰竭的先天性肌病患者中,肌联蛋白激酶结构域的机械应力下降,导致肌肉相关的基因转录下调,最终导致收缩蛋白丢失和肌肉无力。以下的病理生理假设十分有趣:轻-中度COPD患者膈肌的肌联蛋白刚性降低,激酶结构域活性下降,从而导致肌联蛋白和细胞核之间的信号丢失,最终导致肌肉特异性的基因转录下调(Figure 3)。这些病理生理改变能影响收缩蛋白合成,导致膈肌肌球蛋白丢失。
【COPD膈肌无力的病因】
确定COPD膈肌病理性改变的触发点,将会成为未来研究的主要目标。关于膈肌萎缩和无力的触发点和路径,我们提出以下两种假设(Figure 4)。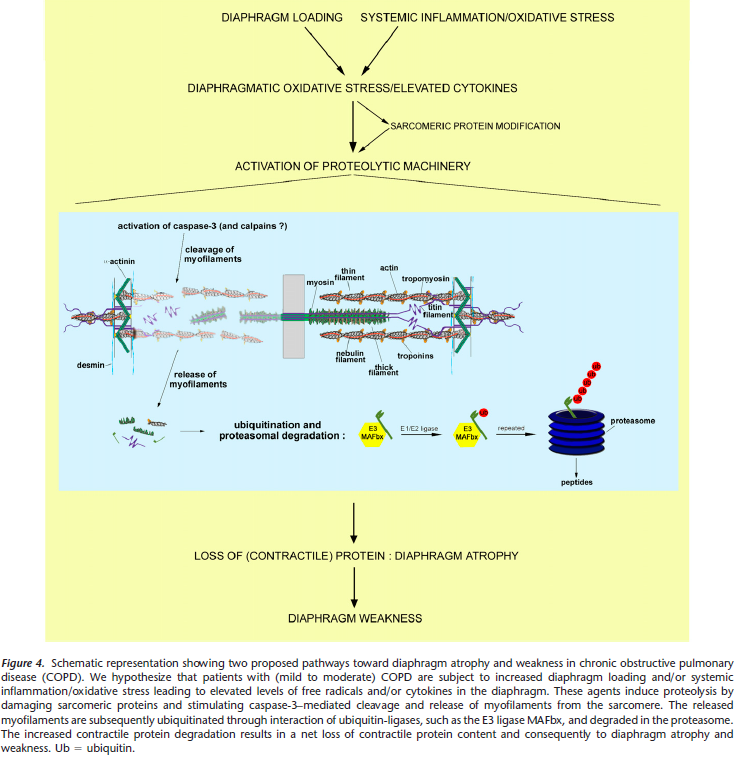
1.长期负荷导致膈肌无力:机械性假说
膈肌收缩活动增加是COPD膈肌改变的潜在触发点,自由基参与其中。自由基可以通过剂量依赖/时间依赖的方式,改变蛋白结构、损伤收缩蛋白功能、激活泛素-蛋白酶体通路。严重COPD的膈肌收缩活性长期增加,可见膈肌的氧化应激反应。但令人惊讶的是,关于轻-中度COPD膈肌收缩活性的研究极少。且极少评估这类患者的氧化应激标记物,当然,氧化蛋白的变化可能太微小而难以发现。因此,将来的研究应确定轻-中度COPD患者的膈肌收缩活性,并确定其是否在膈肌无力中发挥重要作用。
2.全身炎症/氧化应激导致膈肌无力:全身性假设
静息状态下,COPD患者的细胞因子(IL-6、肿瘤坏死因子-α)水平升高,一些研究认为这将导致营养不良。动物实验显示,细胞因子启动横纹肌的损伤过程,损伤收缩蛋白的功能,并通过泛素-蛋白酶体途径刺激蛋白水解。细胞因子可选择性作用于肌球蛋白,启动恶病质相关的肌萎缩。可以推测:轻-中度COPD患者膈肌中细胞因子表达增加,导致肌节损伤、蛋白修饰和降解,但是膈肌和外周肌肉的反应并不相同。因此,了解轻-中度COPD患者细胞因子的情况,将有助于我们了解细胞和分子水平的病因。
【临床角度】
膈肌萎缩在COPD患者膈肌收缩功能障碍中起重要作用。由于膈肌萎缩的病因复杂且存在诸多未知,很难确定治疗目标。但是很可能,泛素-蛋白酶体途径激活,蛋白水解增加,导致肌肉萎缩。因此蛋白酶体活性抑制剂可能具有潜在治疗价值。但是需要注意的是,泛素-蛋白酶体途径只降解损伤和错误折叠的蛋白,抑制蛋白酶体活性可能导致损伤蛋白积累,最终导致细胞死亡。理论上,抑制E3-连接酶而非蛋白酶,是个理想的治疗目标,因为E3-连接酶抑制剂具有很高的底物和组织选择性。目前,尚无泛素-连接酶抑制剂应用于临床。
另一个可能的治疗策略是,阻断肌肉本身的损伤。近期的动物实验证实了阻断筒箭毒碱(肌肉生长抑制剂)对改善肌肉无力的效果。筒箭毒碱是重要的横纹肌生长调节因子,其缺乏可以导致小鼠肌肉含量显著增加。脱乙酰基酶抑制剂可诱导卫星细胞中肌肉生长抑制素拮抗剂follistatin的表达,从而减弱原发基因缺陷导致的形态和功能改变。经过该抑制剂治疗后,卫星细胞中胚胎型肌球蛋白重链表达增加,肌管形成更早且体积增大,肌力产生能力和肌肉形态得到恢复。
参考文献:Ottenheijm CA, Heunks LM, Dekhuijzen PN. Diaphragm muscle fiber dysfunction in chronic obstructive pulmonary disease: toward a pathophysiological concept. Am J Respir Crit Care Med. 2007 Jun 15;175(12):1233-40.